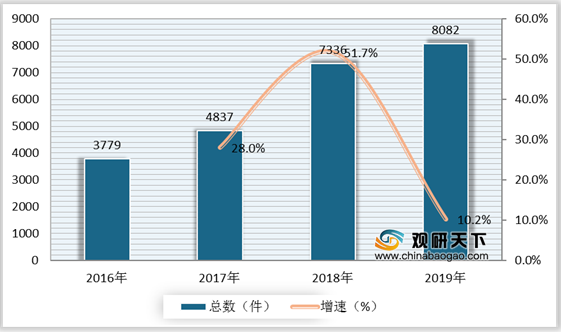
一、总体情况
2019年,我国药审中心受理的8077件药品注册申请中,化学药注册申请受理量为6475件,占2019年全部注册申请受理量的80.2%。
2019年,受理需技术审评的注册申请6199件,较上年增加11.21%,其中化学药注册申请为4937件,较上年增长了10.72%,占全部需技术审评的注册申请受理量的79.64%;中药注册申请257件,较上年降低了14.33%;生物制品注册申请1005件,较上年增长了23.3%。
| 类别 |
2016年 |
2017年 |
2018年 |
2019年 |
| 中药 |
259 |
231 |
300 |
257 |
| 增速(%) |
- |
-10.8 |
29.9 |
-14.3 |
| 化学药 |
3110 |
2979 |
4459 |
4937 |
| 增速(%) |
- |
-4.2 |
49.7 |
10.7 |
| 生物制品 |
410 |
573 |
815 |
1005 |
| 增速(%) |
- |
39.8 |
42.2 |
23.3 |
二、国产创新药受理情况
2019年,药审中心受理国产1类创新药注册申请528件(244个品种),其中受理临床申请503件(228个品种),上市申请25件(16个品种)。按药品类型统计,化学药401件(144个品种),生物制品127件(100个品种),创新药的适应症主要集中在抗肿瘤、抗感染和消化系统疾病领域。
三、进口创新药及原研药受理情况
2019年,药审中心受理5.1类化学药进口原研药注册申请157件(92个品种),受理1类进口创新药注册申请172件(75个品种),创新药的适应症主要集中在抗肿瘤、内分泌和神经系统疾病领域。
四、各类药品注册申请受理情况
(一)化学药注册申请受理情况
2019年,药审中心受理化学药注册申请6475件,其中受理化学药IND申请694件,较2018年增长了51.9%;受理化学药NDA130件,较2018年增长了21.5%;受理仿制药上市申请(ANDA)1047件,较2018年增长了6.6%;受理一致性评价补充申请1038件(308个品种),件数较2018年增长71%。

| 2016年 |
2017年 |
2018年 |
2019年 |
|
| IND申请 |
322 |
40 |
457 |
694 |
| 增速(%) |
|
-87.6 |
1042.5 |
51.9 |
| 验证性临床 |
455 |
89 |
25 |
86 |
| 增速(%) |
|
-80.4 |
-71.9 |
224 |
| NDA |
86 |
75 |
107 |
130 |
| 增速(%) |
|
-12.8 |
42.7 |
21.5 |
| ANDA |
714 |
548 |
982 |
1047 |
| 增速(%) |
|
-23.2 |
19.2 |
6.6 |
| 一致性评价 |
0 |
71 |
607 |
1038 |
| 增速(%) |
|
|
754.9 |
71 |
1.国产、进口化学药IND申请、NDA受理情况
2019年,在化学药IND申请中,受理国产化学药IND申请444件,占比为63.98%;受理进口IND申请250件,占比为36.02%。国产化学药IND申请的适应症主要集中在抗肿瘤、消化系统和抗感染药物领域,进口IND申请的适应症主要集中在抗肿瘤、抗感染药物和神经系统领域。
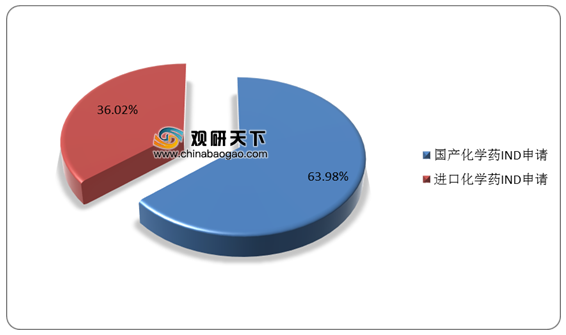
2019年,化学药NDA中,受理国产化学药NDA45件,占比为34.62%;受理进口化学药NDA85件,占比为65.38%。国产化学药NDA的适应症主要集中在抗肿瘤和抗感染药物领域,进口化学药NDA的适应症主要集中在抗肿瘤和神经系统领域。

2.1类化学药创新药受理情况
2019年,药审中心受理1类化学药创新药注册申请573件(219个品种),品种数较2018年增加了39.5%,其中受理IND申请206个品种,较2018年增长了46.1%;受理NDA13个品种,较2018年减少了3个。219个品种的1类化学药创新药注册申请中,国产化学药创新药注册申请为144个品种,进口化学药创新药注册申请为75个品种。

(二)中药注册申请受理情况
2019年,药审中心受理中药注册申请423件,其中受理中药IND申请17件,受理中药NDA3件,受理中药ANDA3件。
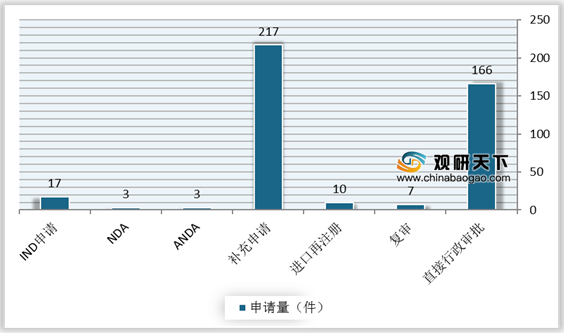
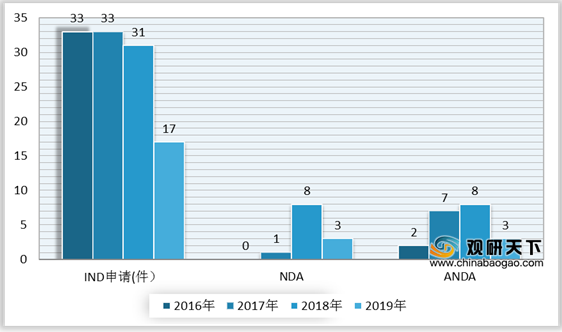
1.中药IND申请受理情况
2019年,在17件中药IND申请(5、6、8类)中,适应症主要集中的治疗领域为消化、呼吸和骨科,占全部中药IND申请的76%。
2.中药新药受理情况
2019年,药审中心受理5-6类中药新药注册申请18件(18个品种,无1-4类中药注册申请),其中中药IND申请15件(15个品种),中药NDA 3件(3个品种),较2018年均有所减少。
(三)生物制品注册申请受理情况
2019年,药审中心受理生物制品注册申请1179件,其中受理生物制品IND申请310件(预防用IND申请7件,治疗用IND申请303件),较2018年增长了4%;受理生物制品NDA124件(预防用NDA7件,治疗用NDA117件),较2018年增长了45.9%。

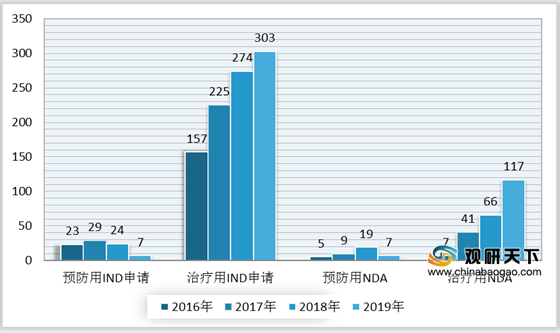
1.I类生物制品创新药受理情况
2019年,药审中心受理1类生物制品创新药注册申请127件(100个品种),件数较2018年增长了3.3%,其中预防用生物制品2件,治疗用生物制品125件。1类生物制品创新药注册申请中,IND申请121件(96个品种),较2018年增长了8%;NDA6件(4个品种,均为治疗用生物制品),较2018年减少了5件。
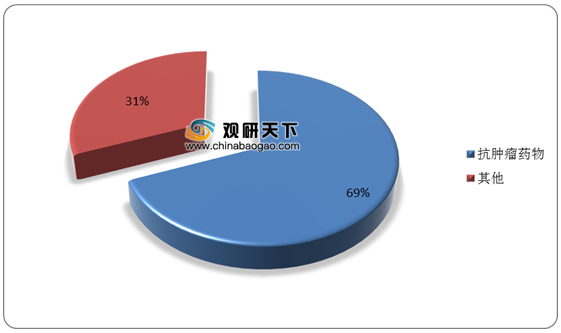
2019年,药审中心受理1类治疗用生物制品IND申请119件(95个品种),适应症主要集中在抗肿瘤治疗领域,占全部1类治疗用生物制品IND申请的69%。
相关行业分析报告参考《2020年中国药品行业分析报告-行业供需现状与未来规划分析》。


【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。